Anvisa interrompe estudo da Coronavac após "evento adverso grave"
Segundo a Anvisa, o fato ocorreu no dia 29 de outubro e que irá analisar os dados para julgar sobre o risco ou benefício da continuidade do estudo da vacina Coronavac.
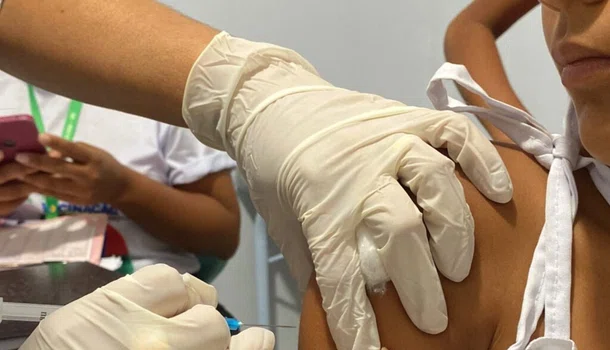
Após ocorrer um “evento adverso grave” durante o estudo realizado com a vacina Coronavac, produzida contra a Covid-19 em parceria com o Instituto Butantan, a Agência Nacional de Vigilância Sanitária (Anvisa) informou que resolveu suspender o estudo da vacina.
Por meio de nota, a Anvisa não explicou qual tipo de evento seria esse, mas afirma que o fato ocorreu no dia 29 de outubro e que irá analisar os dados para julgar sobre o risco ou benefício da continuidade do estudo. Segundo a Anvisa, com a suspenção do estudo a vacina não poderá ser testada em novos voluntários.
“Com a interrupção do estudo, nenhum novo voluntário poderá ser vacinado. A Anvisa reitera que, segundo regulamentos nacionais e internacionais de Boas Práticas Clínicas, os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes”, diz um trecho da nota.
A vacina Coronavac é desenvolvida pela farmacêutica chinesa Sinovac em parceria com o Instituto Butantan, e antes da Anvisa suspender o estudo, a vacina era tida como a mais segura entre as outras que já haviam sido testadas pelo Butantan.
-
Saiba como fazer a prevenção de cinomose canina nos pets
O imunizante, Vanguard Plus, utilizada contra a cinomose e outras doenças está disponível na Clínica-Escola da UNINASSAU Jockey. -
Esperantina alerta para vacinação contra a gripe de pessoas com doenças crônicas
As autoridades de saúde reforçam o apelo sob o lema de que "A vacinação salva vidas!", incentivando os cidadãos a garantirem sua dose para a proteção individual e coletiva de toda a comunidade. -
Hospital Regional Tibério Nunes contará com mais de 300 leitos após obras em Floriano
Conforme a Sesapi, os investimentos em estrutura e ampliação dos serviços ultrapassam R$ 18 milhões. -
Mais de 20 municípios do Piauí são beneficiados com Carreta de Ressonância Magnética
De acordo com a Secretaria de Estado da Saúde do Piauí (Sesapi), o projeto do Ministério da Saúde garante acesso a exames especializados. -
FMS amplia vacinação contra gripe para novos grupos prioritários em Teresina
A FMS ressalta que, a vacina está disponível de segunda a sexta-feira, nos turnos manhã e tarde, em todas as 91 UBS de Teresina.








E-mail
Messenger
Linkedin
Gmail
Tumblr
Imprimir