Covid-19: Wellington encaminha à Anvisa pedido de validação da Pfizer
Segundo Wellington Dias, a Anvisa terá 72 horas para se manifestar sobre essa liberação. Se o prazo acabar e não houver manifestação por parte da Agência, a autorização excepcional fica concedida.
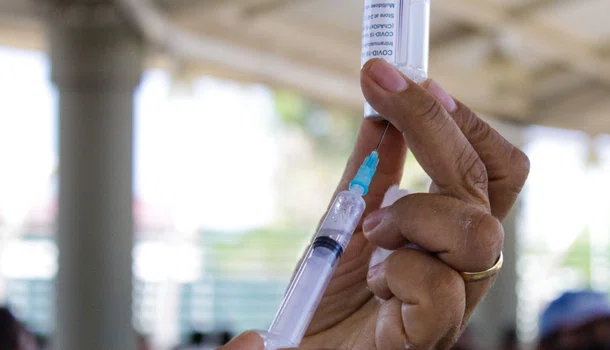
O Governador do Piauí e presidente do Consórcio Nordeste, Wellington Dias, informou nesta quinta-feira (10), que vai encaminhar à Agência Nacional de Vigilância Santiária (Anvisa), o pedido de validação da vacina contra a Covid-19, da Pfizer, após a Food and Drug Administration (FDA), agência reguladora equivalente à Anvisa nos Estados Unidos, emitir um documento confirmando a segurança e eficácia da vacina, na última terça-feira (8).
O relatório detalha informações sobre a eficácia da vacina BNT162b2, desenvolvida pela Pfizer, em parceria com a BioNTech, confirmando a eficácia de 95% da vacina, cerca de sete dias após a aplicação da segunda dose.
De acordo com o presidente, o pedido é feito conforme o previsto na lei nº 13.979, de 6 de fevereiro de 2020, a “Lei Covid”, na qual vacinas contra a doença que conseguirem registros em agências internacionais deverão ser liberadas para uso emergencial no Brasil.
Segundo Wellington Dias, a Anvisa terá 72 horas para se manifestar sobre essa liberação. Se o prazo acabar e não houver manifestação por parte da Agência, a autorização excepcional fica concedida.
Em conjunto, a legislação atual permite que os estados importem e distribuam vacinas contra o novo coronavírus, que ainda não tenham sido registradas pela Anvisa. Para tanto, o imunizante precisa do registro em alguma das seguintes agências reguladoras de saúde: Estados Unidos, Europa, Japão ou China.
Wellington Dias
Anvisa
Consórcio Nordeste
Vacina contra Covid-19
Covid-19
Coronavírus
FMS de Teresina fará 3º mutirão de consultas e exames neste sábado
Segundo a FMS, o mutirão é voltado para pacientes que já estão aguardando consulta pelo Sistema Único de Saúde (SUS) em Teresina, e tem por objetivo reduzir a fila de espera.Mais de 80% dos pacientes do HUT vítimas de acidentes de trânsito são motociclistas
Conforme o hospital, observa-se uma predominância significativa do sexo masculino, representando 74% dos casosApenas 13% do público alvo tomou vacina contra a gripe em Teresina, diz FMS
Até o dia 21 de abril foram aplicadas em Teresina o total de 34.054 doses de vacina contra a gripe, atingindo apenas 13,85% da população alvo (323.616 pessoas).FMS de Teresina imuniza venezuelanos contra a gripe em abrigos
De acordo com a Fundação Municipal de Saúde, a ação aconteceu nesta quinta-feira (18) e visa ampliar as taxas de vacinação neste público alvo.Hospital de Urgência de Teresina faz seleção para Projeto em Fisioterapia
O resultado final será divulgado no dia 07 de junho, com início das atividades previsto para o dia 24 de junho








E-mail
Messenger
Linkedin
Gmail
Tumblr
Imprimir